海洋生态系统正遭受人类活动(例如气候变化)的加速破坏。海洋温度升高导致病原体爆发、有害藻类大量繁殖,并造成珊瑚胁迫。这些都可能对海洋生态系统、人类健康和水产养殖业造成严重后果,构成一个至关重要的“同一健康”问题。监测关键海洋物种能够提供宝贵的信息,但现有方法资源密集、分辨率低且不适用于频繁部署。哈佛大学James J. Collins和Peter Q. Nguyen介绍了一种低成本、可现场部署的 CRISPR 生物传感平台,用于检测海洋生物的 DNA 和 RNA。利用 CRISPR 诊断技术在环境生物监测中的可编程性,展示了该平台在三种与气候相关的指标( 弧菌属、 拟菱形藻属和受热胁迫的珊瑚)上的通用性。便携式 3D 打印处理器和培养箱装置能够直接处理滤膜捕获的样本并进行温度控制。冻干试剂、侧向流动检测、滴管操作和两步多重检测流程,无需实验室仪器即可在 1 小时内获得结果,从而增强了现场检测的便捷性。使用真实病原体和环境海水进行基准测试,证实了该方法对海水的耐受性,并能可靠地检测每滤膜上 10⁸个菌落形成单位的弧菌病原体,相当于每升过滤样品中每微升含有 10²个菌落。这一分散式平台降低了常规监测的门槛,能够对生态系统扰动发出早期预警,同时支持海洋领域的“同一健康”倡议。
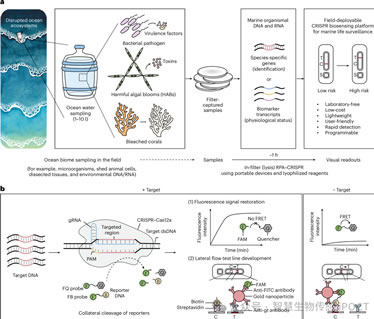
图 1:用于可持续海洋监测的现场可部署 CRISPR 生物传感平台。a . 气候变化和人为污染破坏了海洋生态系统,重塑了海洋生物群落,导致病原体爆发、产生毒素的有害藻华和珊瑚白化。基于 CRISPR 的现场可部署生物监测技术能够实现快速、频繁且用户驱动的海洋健康监测。这可以通过检测指示物种的基因特征并利用生物标志物转录本评估其生理状态来实现。这些传感方式被整合到一个无需实验室的工作流程中,该流程使用低成本、轻便的 3D 打印设备,能够在现场处理和检测海洋物种。b . V 型 CRISPR-Cas12a 诊断的工作原理。Cas12a 在互补的 gRNA 的引导下靶向双链 DNA。靶标识别激活 Cas12a 的非特异性核酸酶活性,从而切割荧光团/淬灭剂标记的探针(FQ 探针,如图 1 所示)或 FAM/生物素标记的探针(FB 探针,如图 2 所示),分别产生荧光或比色 LFA 读数。
来源:传感器专家网



